Ортопедическая хирургия переживает технологическую революцию. На смену стандартным имплантатам массового производства приходят персонализированные протезы, созданные по данным компьютерной томографии конкретного пациента. Аддитивные технологии позволяют изготавливать изделия со сложной геометрией, которые невозможно получить традиционным литьем или механической обработкой.
Титановые сплавы занимают особое место в медицинской имплантологии. Сочетание высокой прочности, низкой плотности и превосходной биосовместимости делает их материалом первого выбора для челюстно-лицевой хирургии, ортопедии и нейрохирургии. Возможность создавать пористые структуры, имитирующие губчатую кость, открывает новые горизонты в восстановительной медицине.
Эта статья раскрывает полную картину применения 3D-печати титановых имплантатов: от характеристик порошков и технологий производства до реальных клинических кейсов с результатами многолетнего наблюдения за пациентами.
Почему титан стал стандартом медицинской имплантологии
Титан обладает уникальным сочетанием свойств, которое делает его незаменимым в хирургии. Металл формирует на поверхности тонкую оксидную пленку, обеспечивающую исключительную коррозионную стойкость в агрессивной среде человеческого организма. Биологическая инертность титана подтверждена десятилетиями клинической практики — аллергические реакции на этот металл встречаются крайне редко.
Удельная прочность титана превосходит показатели нержавеющей стали при меньшей массе, что критично для имплантатов, которые пациент будет носить всю жизнь. Модуль упругости титановых сплавов, хотя и превышает показатели костной ткани, значительно ближе к ним, чем у кобальт-хромовых сплавов. Это снижает риск резорбции кости вокруг имплантата из-за неравномерного распределения нагрузки.
Ti6Al4V: рабочая лошадка ортопедии

Сплав Ti6Al4V (Grade 5) содержит 6% алюминия и 4% ванадия, которые стабилизируют соответственно альфа- и бета-фазы титана. Такое сочетание обеспечивает оптимальный баланс между прочностью и пластичностью, позволяя имплантату выдерживать как статические, так и циклические нагрузки.
Изделия, напечатанные методом лазерного сплавления порошка, демонстрируют предел прочности свыше 1000–1200 МПа и предел текучести выше 900 МПа. Эти показатели превосходят характеристики литых или кованых аналогов благодаря мелкозернистой микроструктуре, формирующейся при быстром охлаждении расплавленного металла. Минимальные требования стандарта ASTM F136 составляют 827–830 МПа по пределу прочности и 758–760 МПа по пределу текучести — современное оборудование для 3D-печати стабильно превышает эти нормы.
Grade 23: золотой стандарт для ответственных имплантатов
Версия сплава с экстра-низким содержанием примесей внедрения (Ti6Al4V ELI, Grade 23) разработана специально для медицинских применений. Кислород, азот, углерод и водород в титане располагаются в междоузлиях кристаллической решетки, и их избыток приводит к охрупчиванию металла. В Grade 23 содержание кислорода ограничено 0,13% против 0,20% в стандартном Grade 5, железа — 0,25% против 0,40%, азота — 0,03%.
Строгий контроль примесей обеспечивает превосходную трещиностойкость — критически важное свойство для имплантатов, работающих в условиях циклических нагрузок. Протезы тазобедренного сустава, зубные штифты, спинальные имплантаты подвергаются миллионам нагрузочных циклов за годы эксплуатации. Любая микротрещина в менее чистом материале способна привести к катастрофическому разрушению. Grade 23 также демонстрирует повышенную пластичность — способность деформироваться под экстремальной нагрузкой без внезапного разрушения.
Производство порошков медицинского класса
Качество титанового порошка напрямую определяет эксплуатационные характеристики готового имплантата. Для аддитивного производства требуются частицы строго сферической формы с минимальным содержанием примесей и узким гранулометрическим распределением.
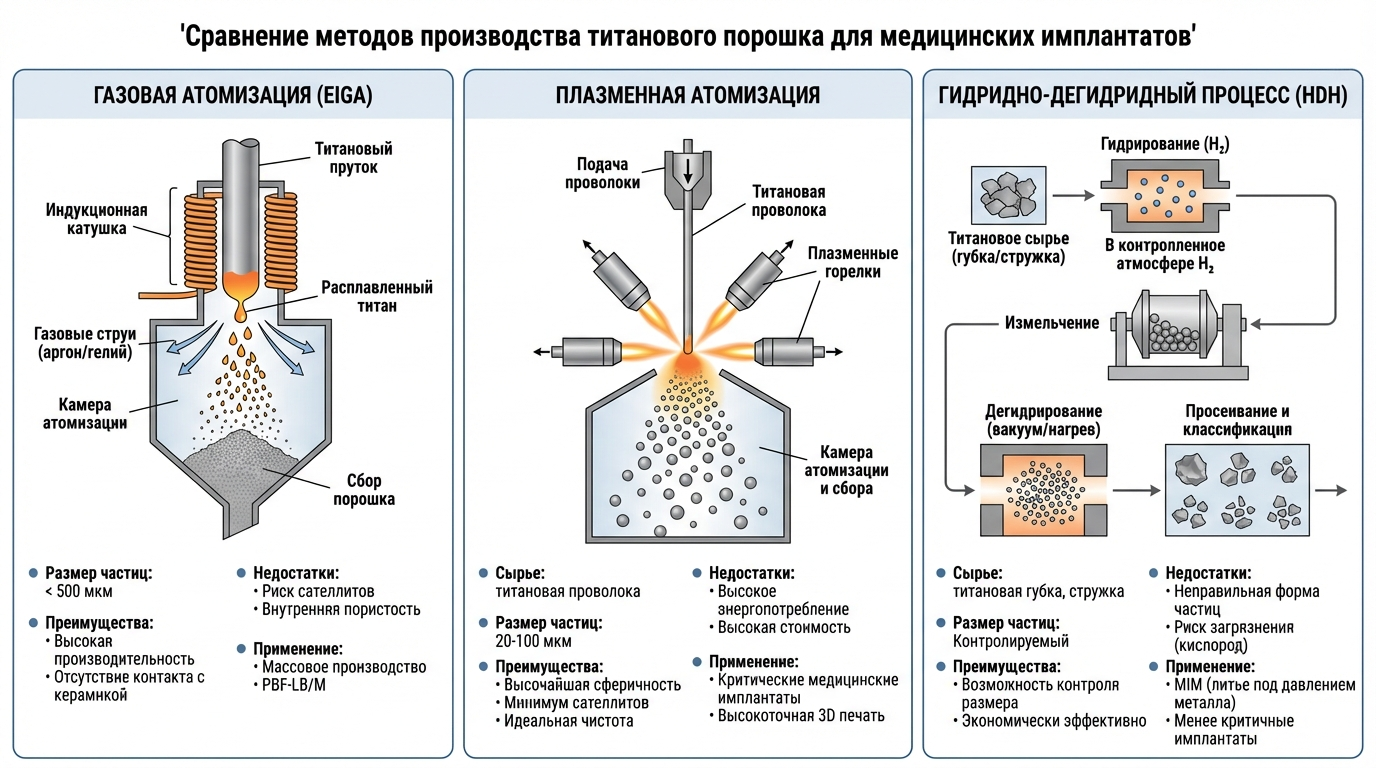
Газовая атомизация: массовое производство
Традиционный метод получения металлических порошков основан на распылении расплавленного металла струей инертного газа под высоким давлением. Исходный материал плавится в вакуумной индукционной печи, после чего расплав подается через нагреваемое сопло и разбивается на мелкие капли, застывающие в свободном падении.
Газовая атомизация позволяет получать частицы в широком диапазоне размеров (менее 500 мкм) и обеспечивает высокую производительность. Однако для этого метода характерно образование частиц-сателлитов — мелких капель, прилипающих к более крупным. Сателлиты ухудшают текучесть порошка и могут вызвать дефекты при нанесении слоев в 3D-принтере. Также существует риск загрязнения керамикой от сопла и захвата аргона внутрь частиц, что создает внутреннюю пористость.
Усовершенствованная версия — электродно-индукционная газовая атомизация (EIGA) — исключает контакт расплава с керамикой. Титановый стержень плавится индукционной катушкой, капая непосредственно в зону распыления. Это значительно повышает чистоту порошка.
Плазменная атомизация: чистота и сферичность
В качестве сырья для плазменной атомизации используется титановая проволока, которая плавится высокоскоростными плазменными горелками и одновременно разбивается на капли. Метод обеспечивает высочайшую чистоту и отличную сферичность частиц с минимальным количеством сателлитов.
Основное ограничение — высокая стоимость из-за дороговизны проволочного сырья. Кроме того, использовать можно только те сплавы, которые производятся в виде проволоки. Для медицинских применений, где стоимость материала вторична по сравнению с качеством, плазменная атомизация считается оптимальным выбором для мелких фракций порошка.
PREP: идеальная геометрия без внутренних дефектов
Плазменный процесс с вращающимся электродом (Plasma Rotating Electrode Process) представляет собой уникальную технологию. Быстро вращающийся титановый стержень плавится плазменной горелкой в среде гелия. Под действием центробежной силы капли расплава разлетаются от электрода и застывают в полете.
Порошки PREP отличаются идеальной сферичностью и полным отсутствием внутренних газовых пор, поскольку в процессе не используется газ под высоким давлением. Метод минимизирует количество примесей и сателлитов. Ограничение — частицы обычно крупнее (100–300 мкм), что подходит для электронно-лучевого сплавления, но может быть избыточным для лазерных систем, требующих мелкую фракцию.
Требования к характеристикам порошка
Для лазерного сплавления (PBF-LB/M) используются мелкие порошки в диапазоне 20–100 мкм, обеспечивающие высокую точность и качество поверхности. Электронно-лучевая плавка (PBF-EB/M) допускает более крупные частицы 40–150 мкм, что способствует стабильности процесса в вакууме. Для технологии прямой наплавки (DED) применяются частицы от 50 до 150 мкм и выше.
Сферическая форма обеспечивает хорошую текучесть порошка при нанесении слоев и высокую плотность упаковки. Текучесть измеряется с помощью калиброванных воронок Холла или Карни — порошок должен свободно высыпаться через отверстие диаметром 2,5–5 мм. Низкая текучесть приводит к образованию дефектов в слое, несплавлениям и снижению прочности готового изделия.
Технологии 3D-печати титановых имплантатов
Современное аддитивное производство медицинских изделий базируется на нескольких принципиально различных технологиях, каждая из которых имеет свои преимущества и области применения.
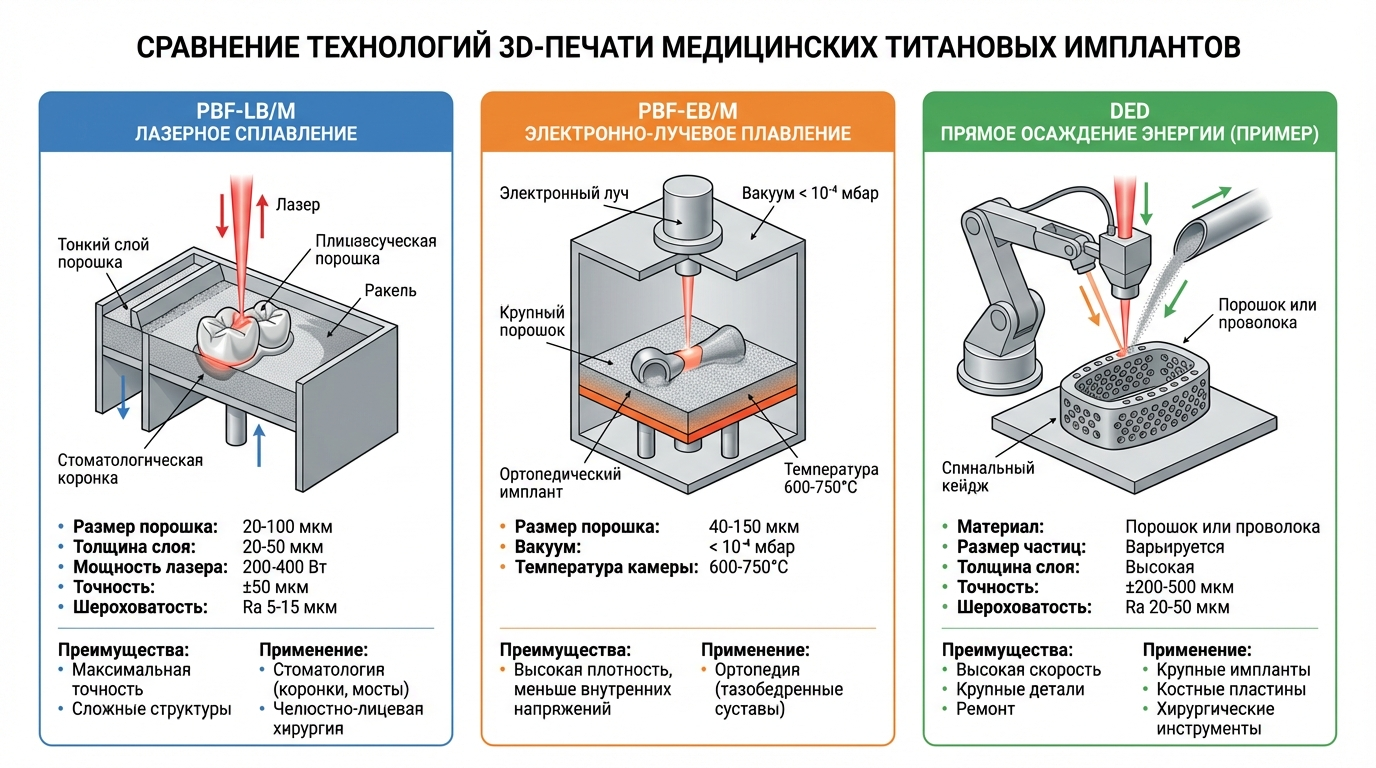
Лазерное сплавление порошкового слоя (PBF-LB/M)
Технология селективного лазерного сплавления (SLM/DMLS) обеспечивает максимальную точность и качество поверхности среди всех методов металлической 3D-печати. Тонкий слой порошка (20–50 мкм) наносится на рабочую платформу, после чего лазер мощностью 200–400 Вт выборочно сплавляет частицы по заданному контуру. Платформа опускается на толщину слоя, наносится новая порция порошка, процесс повторяется до полного построения детали.
Точность лазерного сплавления достигает ±50 мкм, что критично для стоматологических коронок, мостов и других мелких прецизионных изделий. Шероховатость поверхности составляет Ra 5–15 мкм в зависимости от режимов печати. Технология позволяет создавать сложнейшие внутренние структуры, включая пористые скаффолды для врастания кости.
Электронно-лучевое сплавление (PBF-EB/M)
Процесс EBM происходит в глубоком вакууме (менее 10⁻⁴ мбар) с использованием электронного пучка вместо лазера. Высокая температура в камере построения (600–750°C для титана) обеспечивает важное преимущество — минимальные остаточные напряжения в готовом изделии.
При лазерном сплавлении локальный нагрев и быстрое охлаждение создают в металле внутренние напряжения, требующие последующей термообработки. Электронно-лучевая плавка, благодаря равномерному прогреву всей камеры, позволяет получать детали с существенно меньшим уровнем напряжений. Это особенно важно для крупных ортопедических имплантатов — протезов тазобедренного сустава, спинальных кейджей.
Вакуумная среда исключает окисление титана в процессе печати. Метод допускает использование более крупных фракций порошка (45–150 мкм), что упрощает логистику и снижает стоимость сырья.
Прямая наплавка металла (DED)
Технология направленного энергетического осаждения отличается от порошковых методов подачей материала непосредственно в зону действия лазера или электронного пучка. Порошок или проволока плавятся и наносятся на подложку, формируя деталь слой за слоем.
DED незаменим для ремонта дорогостоящих имплантатов и создания изделий с градиентной структурой — например, с переменной пористостью по толщине. Производительность наплавки существенно выше, чем у порошковых методов, но точность и качество поверхности уступают.
Пористые структуры: ключ к успешной остеоинтеграции
Традиционные металлические имплантаты имеют гладкую или текстурированную поверхность, которая обеспечивает механическую фиксацию, но не стимулирует врастание кости. Аддитивные технологии открыли возможность создания анизотропно-пористых структур — скаффолдов, имитирующих архитектуру губчатой кости.
Оптимальная архитектура пор
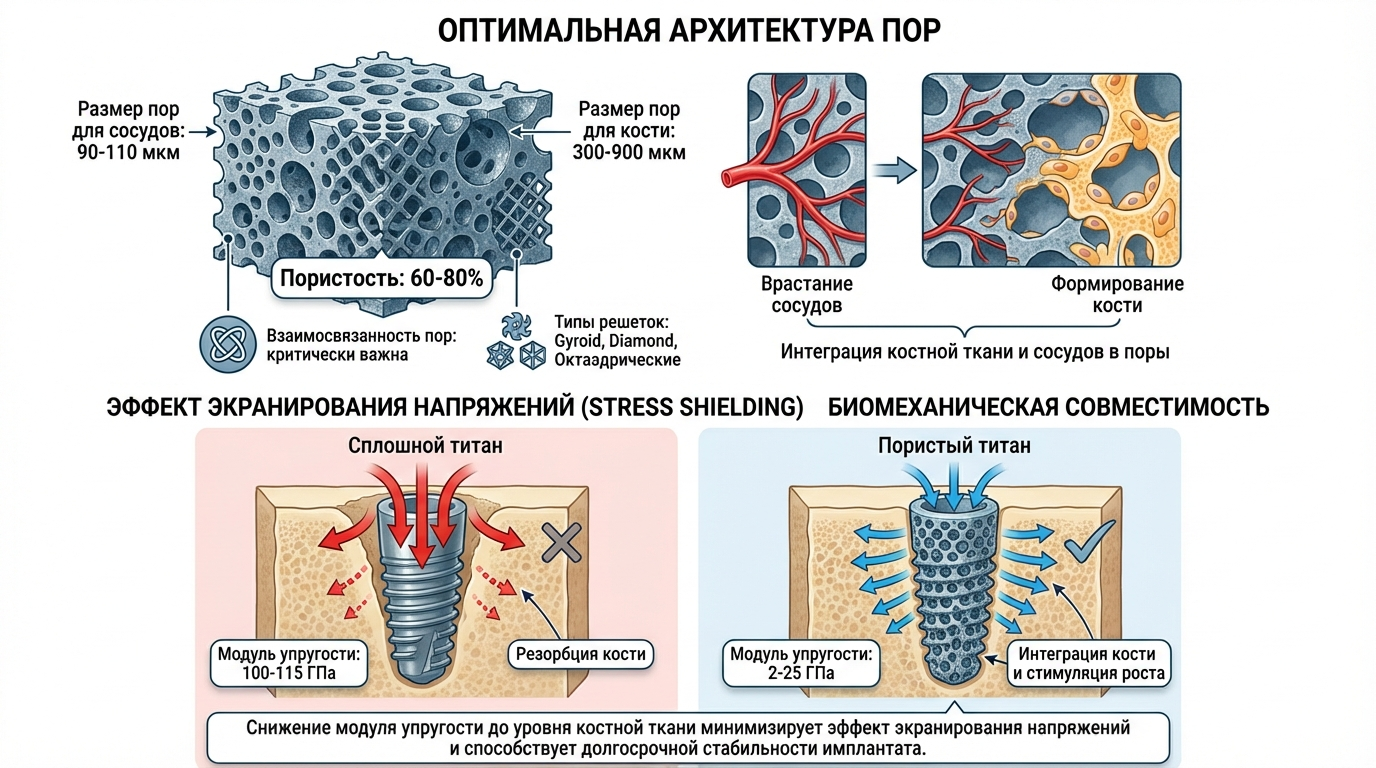
Исследования показывают, что оптимальный размер пор для остеоинтеграции составляет 90–110 мкм для начального прорастания сосудов и 300–900 мкм для формирования костной ткани. Пористость 60–80% обеспечивает баланс между биологической активностью и механической прочностью. Взаимосвязанность пор критически важна — изолированные полости не участвуют в остеогенезе.
Форма пор также имеет значение. Кубические и октаэдрические решетки (типа Gyroid, Diamond) обеспечивают изотропное распределение нагрузки и стимулируют равномерное врастание кости во всех направлениях. Проектирование таких структур требует специализированного программного обеспечения для топологической оптимизации.
Снижение эффекта экранирования напряжений
Сплошной титан имеет модуль упругости 100–115 ГПа, тогда как кортикальная кость — всего 10–30 ГПа. Такое несоответствие приводит к эффекту экранирования напряжений (stress shielding): жесткий имплантат принимает на себя основную нагрузку, лишая окружающую кость физиологического стимула. Результат — постепенная резорбция и ослабление фиксации.
Пористые структуры позволяют снизить эффективный модуль упругости имплантата до 1–5 ГПа, приближая его к показателям губчатой кости. Нагрузка распределяется между имплантатом и окружающей тканью, сохраняя естественный остеогенез. Врастающая костная ткань дополнительно укрепляет соединение, превращая имплантат в интегрированную часть скелета.
Экономия материала
Производство традиционных ортопедических имплантатов методом фрезерования из цельной заготовки сопровождается потерей до 90% дорогостоящего титана в виде стружки. 3D-печать использует материал только там, где он необходим. Для коленных имплантатов экономия достигает 80%. При стоимости порошка Ti6Al4V ELI свыше $300 за килограмм это обеспечивает существенное снижение себестоимости производства.
Создание индивидуального имплантата: от снимка до операционной
Процесс разработки персонализированного протеза включает несколько последовательных этапов, каждый из которых требует специализированного программного обеспечения и экспертизы.
Медицинская визуализация
Исходными данными служат снимки компьютерной или магнитно-резонансной томографии в формате DICOM. Для ортопедических имплантатов обычно достаточно КТ с шагом сканирования 0,5–1 мм. Качество исходных данных напрямую влияет на точность будущего изделия — артефакты от металлических объектов, недостаточное разрешение или неполный охват области интереса приведут к ошибкам на последующих этапах.
Сегментация и 3D-реконструкция
Специализированное программное обеспечение (Materialise Mimics, 3D Slicer, OsiriX) выделяет костную ткань из массива томографических данных и создает трехмерную модель анатомической структуры. Для реконструктивных операций применяется техника зеркального отображения: если дефект затрагивает одну сторону тела, здоровая сторона служит шаблоном для восстановления симметрии.
Проектирование имплантата
Инженер совместно с хирургом определяет границы резекции, точки фиксации и функциональные требования к протезу. Топологическая оптимизация позволяет создать конструкцию с минимальной массой при заданной прочности. Зоны контакта с костью проектируются пористыми для оссеоинтеграции, нагруженные участки остаются сплошными.
Финальная модель экспортируется в формат STL для 3D-печати. Перед производством проводится виртуальная примерка — наложение модели имплантата на анатомию пациента для верификации посадки.
Печать и постобработка
Изготовление имплантата занимает от нескольких часов до суток в зависимости от размера и сложности. После печати изделие отделяется от платформы построения, удаляются поддерживающие структуры. Термическая обработка снимает остаточные напряжения и стабилизирует микроструктуру.
Для медицинских изделий критически важна очистка от остатков порошка. Пористые структуры промываются в ультразвуковой ванне, продуваются сжатым воздухом, проходят многократные циклы очистки. Любые застрявшие частицы способны вызвать воспалительную реакцию после имплантации.
Стерилизация проводится стандартными методами — автоклавирование, гамма-облучение или обработка этиленоксидом. Упакованный имплантат поступает в операционную готовым к установке.
Клинические кейсы: реальные результаты применения
Накопленный опыт использования 3D-печатных титановых имплантатов охватывает тысячи пациентов по всему миру. Ниже представлены характерные примеры из различных областей хирургии.
Реконструкция нижней челюсти
Пациент 63 лет поступил с обширной амелобластомой левой половины нижней челюсти. Предоперационное планирование включало КТ-сканирование и создание виртуальной модели черепа. Индивидуальный титановый протез был спроектирован методом зеркального отображения здоровой стороны с низким профилем для минимизации риска инфекции и отверстиями для реаттачмента мышц.
Операция прошла без осложнений — протез обеспечил идеальную посадку. Пациент был выписан через 5 дней. При контрольном осмотре через 2 года функция челюсти полностью восстановлена, эстетический результат удовлетворительный, признаков инфекции или расшатывания имплантата не выявлено.
В другом случае 53-летнему мужчине установили титановый имплантат челюсти с предварительно смонтированными дентальными имплантатами. Такой подход позволил сократить количество операций и обеспечить немедленную реабилитацию окклюзии. Год наблюдения не выявил инфекционных осложнений.
Сегментарные дефекты костей конечностей
Восстановление массивных потерь костной ткани (более 4 см) бедренной или большеберцовой кости после травм и инфекций традиционно считается сложнейшей задачей ортопедии. Серия из 6 клинических случаев продемонстрировала эффективность комбинации индуцированной мембраны (техника Масквелета) и индивидуального трабекулярного титанового скаффолда.
Пациенты начинали частичную нагрузку на конечность немедленно или в течение 7 дней после операции. Полная нагрузка разрешалась в среднем через 25–30 дней в зависимости от болевого синдрома и восстановления мышечной силы. Рентгенологические признаки начальной интеграции фиксировались на 60-й день, полное костное сращение подтверждалось КТ к 150-му дню. Возвращение к обычной активности занимало в среднем 227 дней.
Краниопластика
Восстановление дефектов свода черепа после травм или удаления опухолей требует точного воспроизведения сложной кривизны костей. Титановые сетки, изготовленные методом лазерного сплавления, обеспечивают превосходную посадку при минимальном весе.
Применение техники зеркального отображения для симметричной реконструкции значительно сокращает время операции — хирургу не приходится подгонять стандартную пластину под индивидуальную анатомию. Пористая структура сетки способствует врастанию тканей и надежной фиксации без дополнительных винтов в некоторых случаях.
Спинальные имплантаты
Системы межтелового спондилодеза CVPI (шейный отдел) и TVPI (грудной отдел) демонстрируют преимущества анизотропно-пористых структур. Шероховатая открытопористая поверхность способствует оссеоинтеграции без необходимости использования костного цемента или дополнительных пластин.
Для пациентки 15 лет с идиопатическим сколиозом 3D-печать использовалась для создания хирургических шаблонов, направляющих точную установку педикулярных винтов. Такой подход минимизирует риск повреждения спинного мозга и нервных корешков при коррекции деформации позвоночника.
Индивидуальные межпозвонковые эндопластины, изготовленные методом DMLS, достигают точности изготовления 0,37 мм — достаточной для надежной посадки в межтеловое пространство.
Стандарты и сертификация медицинских имплантатов
Производство и применение 3D-печатных титановых имплантатов регулируется строгой системой стандартов, обеспечивающих безопасность пациентов.
Международные требования
Система менеджмента качества производителя должна соответствовать ISO 13485 — международному стандарту для медицинских изделий. Этот документ регламентирует все этапы жизненного цикла продукции от проектирования до послепродажного мониторинга.
Титановый сплав Ti6Al4V ELI для хирургических имплантатов должен соответствовать ASTM F136, определяющему химический состав, механические свойства и методы испытаний. Для порошковых материалов применяется ASTM F3001, описывающий требования к характеристикам частиц.
Готовые изделия класса риска IIb и III требуют сертификации CE в Европе или clearance FDA в США. Для персонализированных имплантатов, изготавливаемых по индивидуальному заказу, существуют упрощенные процедуры — так называемые Custom Device Exemptions.
Трассируемость и документация
Каждая партия порошка сопровождается сертификатом анализа с указанием химического состава, гранулометрического распределения, плотности и текучести. Производитель имплантатов обязан обеспечить полную трассируемость — возможность установить, из какой партии сырья изготовлено конкретное изделие.
Документация на персонализированный имплантат включает исходные данные визуализации, отчет о проектировании, протокол печати с параметрами процесса, результаты контроля качества и заключение о стерилизации. Вся информация хранится в течение установленного срока для возможного расследования в случае осложнений.
Перспективы развития технологии
Аддитивное производство медицинских имплантатов продолжает стремительно развиваться, открывая новые возможности для персонализированной медицины.
Биоактивные и антибактериальные покрытия
Следующее поколение имплантатов объединит несущую титановую структуру с функциональными покрытиями. Гидроксиапатит и биоактивные стекла ускоряют остеоинтеграцию, создавая на поверхности слой, химически близкий к минеральной фазе кости. Серебросодержащие и медьсодержащие покрытия обеспечивают антибактериальный эффект, снижая риск периимплантатной инфекции.
Интеграция с искусственным интеллектом
Алгоритмы машинного обучения уже применяются для автоматической сегментации томографических данных, сокращая время подготовки модели с часов до минут. Генеративный дизайн позволяет оптимизировать геометрию имплантата по заданным критериям — минимальный вес, максимальная прочность, оптимальное распределение напряжений. В перспективе AI будет предсказывать долгосрочные результаты имплантации на основе анализа анатомических особенностей пациента.
Биорезорбируемые материалы
Для некоторых применений — фиксация переломов у детей, временная стабилизация — идеальным решением были бы имплантаты, постепенно рассасывающиеся по мере заживления кости. Магниевые сплавы и полилактидные композиты находятся на стадии клинических испытаний. 3D-печать таких материалов позволит создавать временные скаффолды, полностью замещающиеся собственной костной тканью пациента.
Часто задаваемые вопросы
Каковы преимущества пористых титановых имплантатов перед сплошными?
Пористые структуры обеспечивают остеоинтеграцию — врастание костной ткани в поры размером 300–900 мкм. Это создает надежную биологическую фиксацию без необходимости использования винтов или костного цемента. Дополнительно пористость снижает эффективный модуль упругости имплантата, предотвращая атрофию окружающей кости из-за эффекта экранирования напряжений.
Почему Ti6Al4V ELI предпочтительнее стандартного Ti6Al4V?
Grade 23 имеет строго контролируемое содержание примесей внедрения — кислорода, азота, водорода. Это обеспечивает превосходную трещиностойкость и пластичность, критически важные для имплантатов, работающих в условиях циклических нагрузок миллионы раз за срок службы.
Сколько времени занимает изготовление индивидуального имплантата?
От получения данных КТ до готового стерильного изделия проходит в среднем 2–5 дней. В экстренных случаях возможно сокращение до 24–48 часов. Основное время занимает не печать (несколько часов), а проектирование, согласование с хирургом и постобработка.
Безопасны ли 3D-печатные титановые имплантаты?
Да, при условии соблюдения стандартов производства и сертификации. Титановые имплантаты проходят строгие испытания на биосовместимость, механическую прочность и стерильность. Клинический опыт применения насчитывает тысячи успешных операций с многолетним периодом наблюдения.
Как долго служит 3D-печатный титановый имплантат?
При правильной установке и отсутствии осложнений — десятилетия. Пористая структура обеспечивает интеграцию с костью, делая имплантат частью скелета. Многие пациенты живут с титановыми протезами всю жизнь без необходимости ревизионных вмешательств.
Заключение
Аддитивное производство титановых имплантатов — это не экспериментальная технология, а состоявшаяся клиническая практика с доказанной эффективностью. Возможность создавать персонализированные протезы с оптимальной геометрией и пористой структурой для врастания кости открывает новую страницу в восстановительной хирургии.
Сочетание высокопрочных титановых сплавов медицинского класса, прецизионных технологий лазерного и электронно-лучевого сплавления, современных методов проектирования обеспечивает результаты, недостижимые при традиционном производстве. Пациенты получают имплантаты, идеально соответствующие их анатомии, с сокращенным временем реабилитации и улучшенными долгосрочными прогнозами.
Развитие биоактивных покрытий, интеграция с искусственным интеллектом и появление биорезорбируемых материалов обещают сделать персонализированную имплантологию еще более эффективной и доступной в ближайшие годы.




